Lo scopo di questo articolo è di offrire una rapida riflessione in ottica lotta all’AMR, riportando sinteticamente gli aggiornamenti sostanziali, senza sostituire un’attenta e dettagliata lettura integrale di questo masterpiece per la Medicina Generale.
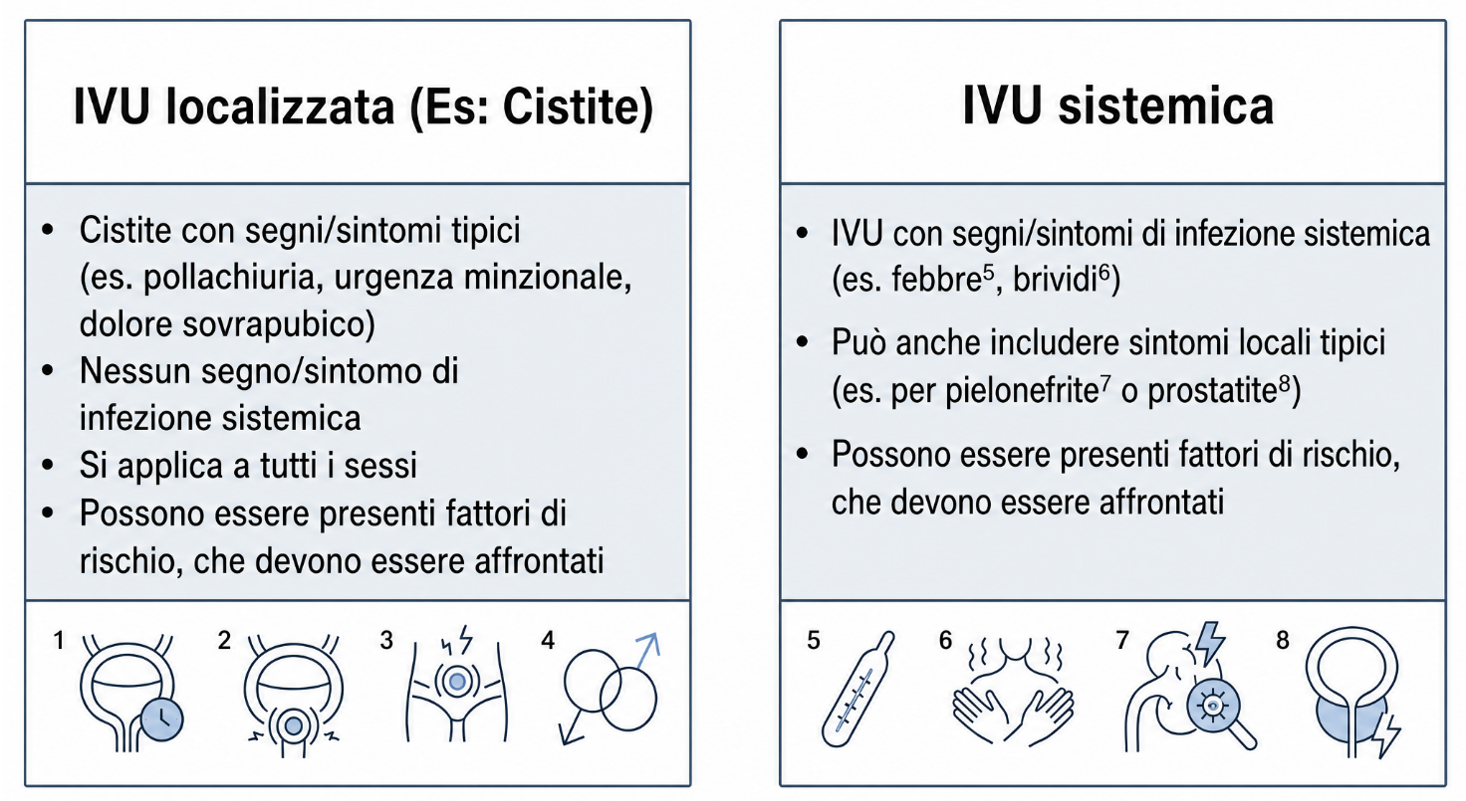
Le recenti linee guida pubblicate a marzo 2026 da parte dell’EAU1, confermano le precedenti classificazioni, rafforzando le precedenti del 2025, assecondate dal consensus dato dalle IDSA 20252:
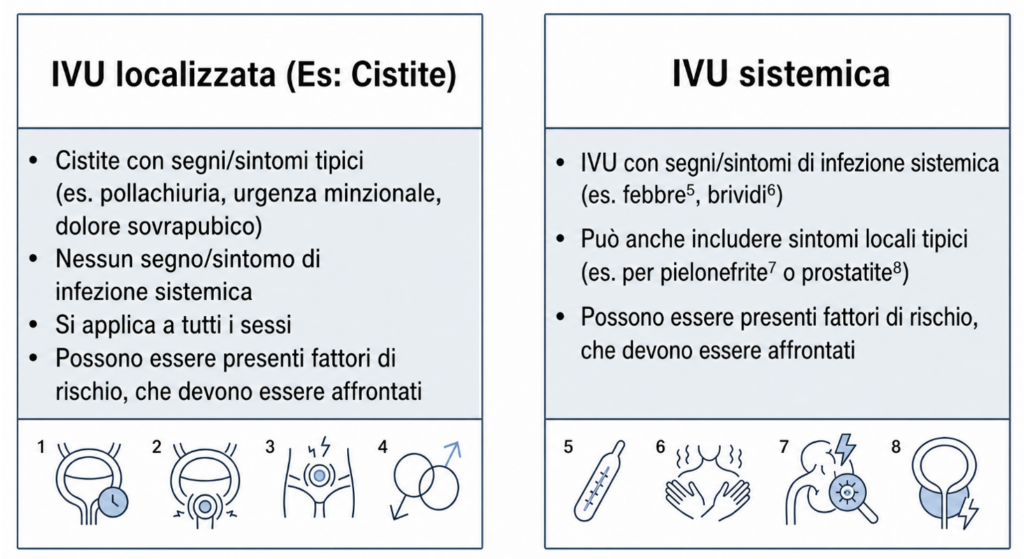
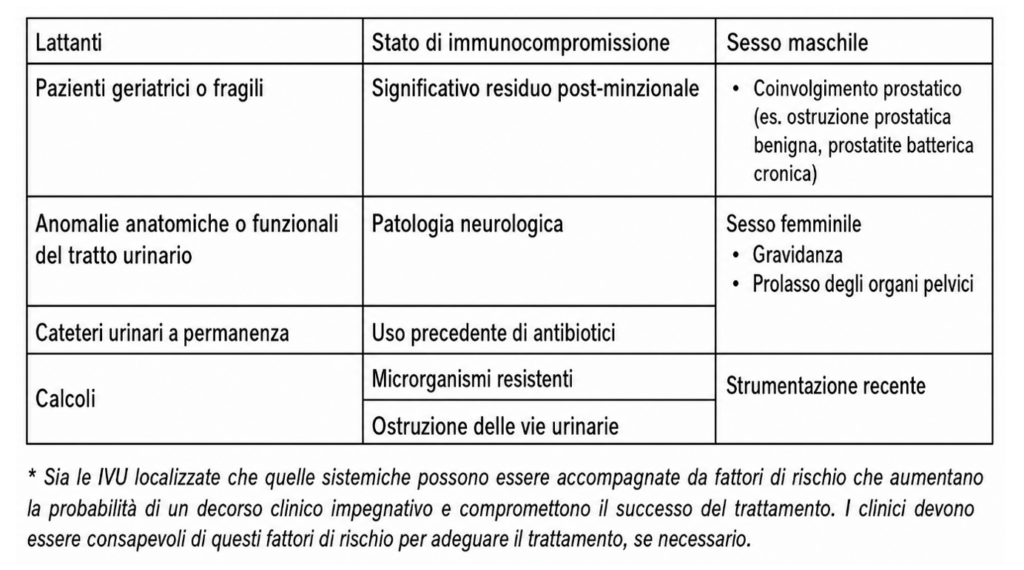
Tale classificazione lascia al clinico la possibilità interpretativa, sulla base dei plurimi fattori di rischio riconosciuti e tabellati, lasciando una sfida molto avvincente su come questi possano spostare l’asticella verso un atteggiamento più aggressivo.
Quando eseguire un’urinocoltura (U/C)?
Urinocoltura si, urinocoltura nò, mindset del m’ama non m’ama, rimane ad oggi una domanda a cui le recenti guidelines si settano in maniera sempre convinta nel confermare la necessità di U/C nel sospetto di forme sistemiche, nel caso di procedure urologiche che violano la mucosa, donne in gravidanza3 , forme ricorrenti, mancata risoluzione clinica dopo 4 settimane di trattamento e donne con sintomi atipici.
Il trattamento antibiotico empirico nelle UTI localizzate
Riscopriamo due molecole che vengono selezionate in prima linea di trattamento:
-Pivmecillina, molecola dotata di altissima affinità recettoriale per la penicillin binding protein 2 (PBP-2)4, con alta tollerabilità ed efficacia (si ricorda inoltre che il farmaco approvato in Italia, è prescrivibile solo in fascia C)
-Nitroxolina5, attualmente non commercializzata in Italia, con attività batteriostatica verso E.Coli
Per il resto, come riportato in schema, si confermano le indicazioni proposte nel 2025:
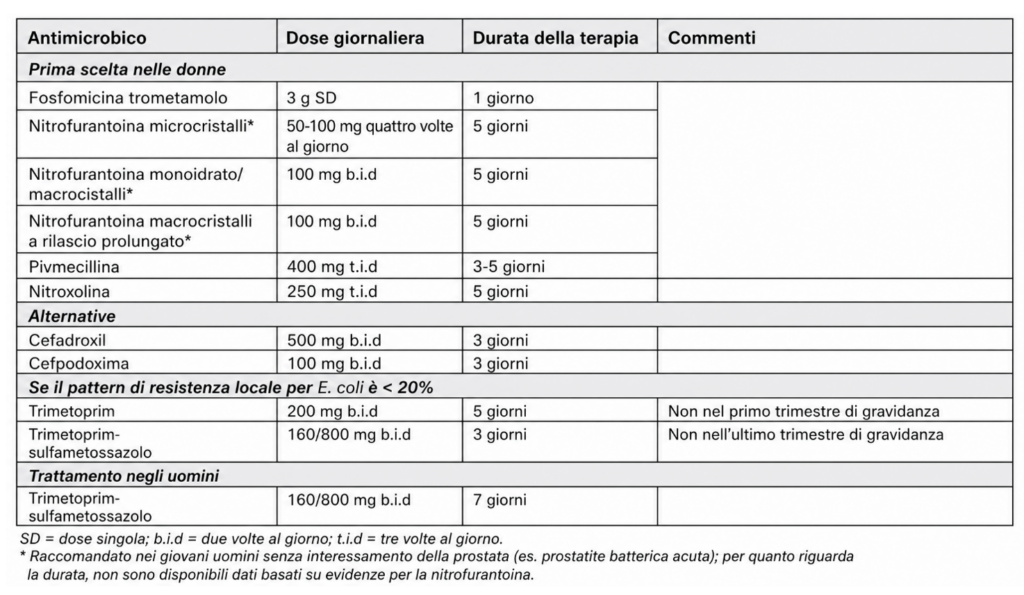
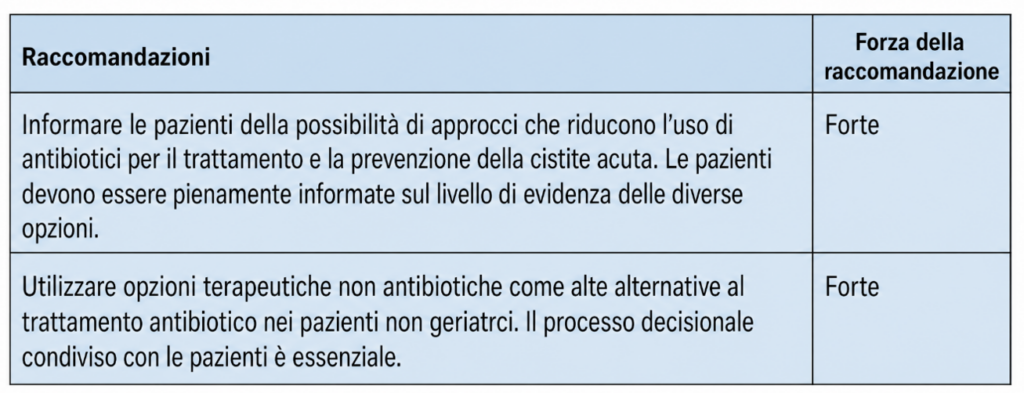
Possibilità terapeutiche alternative IVU Localizzate?
Da sempre discussa la possibilità d’intervenire in maniera alternativa, non farmacologica, i recenti update ci confermano la possibilità in casi selezionati, di evitare la tp antibiotica.
Scorrendo velocemente le recenti indicazioni, si evince la possibilità di trattare con livelli d’evidenza elevati 1A, una combinazione di Xioglucano, Ibisco e Propoli, mentre rimane molto contradditorio (LE 2), l’utilizzo del D-Mannosio, seppur questo venga comunque sostenuto come valido nella Cochrane pubblicata nel 2023, ove viene confermato il suo utilizzo nelle forme recidivanti ed in alcuni specifici setting, molto ricorrenti in Medicina Generale come ad esempio nel bambino e nel paziente sottoposto ad operazioni che coinvolgono la vescica6.
Si ricorda come l’apporto idrico vada portato sopra a 1.5 l/die in corso d’infezione per garantire una vera e propria azione di pulizia meccanica sulla vescica, ma anche per la prevenzione delle forme recidivanti.
Ulteriori considerazioni possiamo estrapolarle dalla recente meta-analisi di Xiong7, l’efficacia dell’utilizzo del succo di Cranberries contenente proantocianidine (PACS), va contestualizzata alla durata 12-24 settimane e nella posologia non inferiore a 36 g/die
Appare centrale il ruolo del clinico nel processo di empowerment del paziente, con il quale vanno stabilite le strategie terapeutiche in maniera sartoriale.

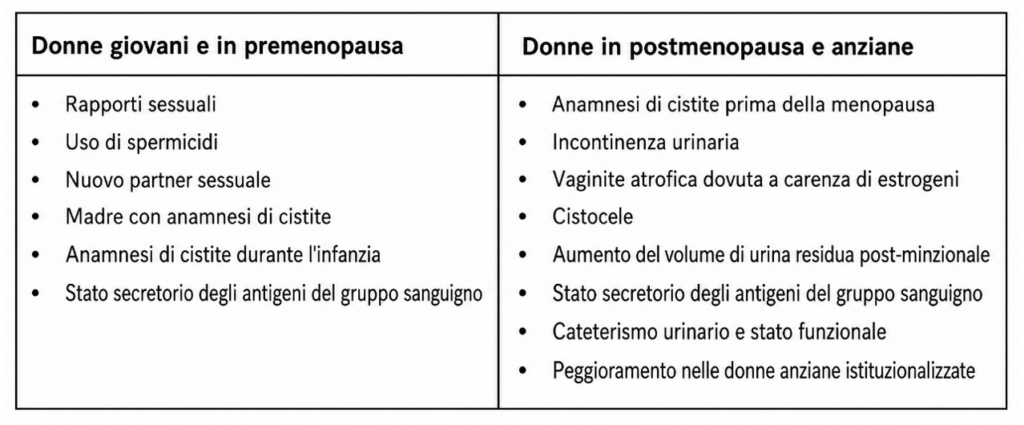
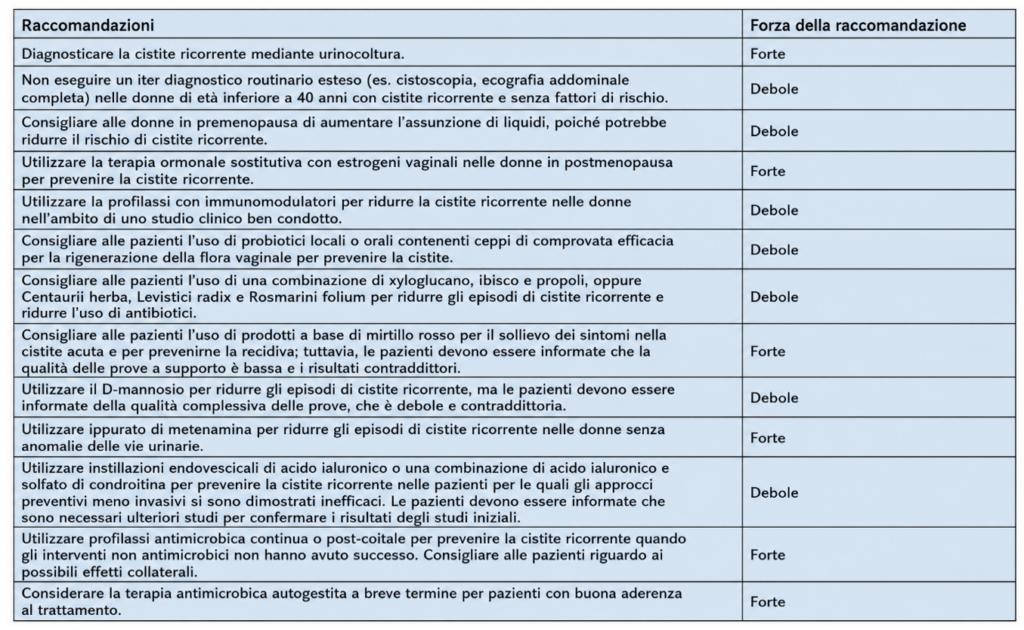
Aggiornamenti nelle forme recidivanti?
Dalla definizione, almeno 2 episodi negli ultimi 6 mesi, oppure tre episodi nell’ultimo anno, alle terapie, non ci sono particolari novità, rispetto alle EAU 2025; si riporta in calce il sommario delle evidenze, e i fattori di rischio addizionali.
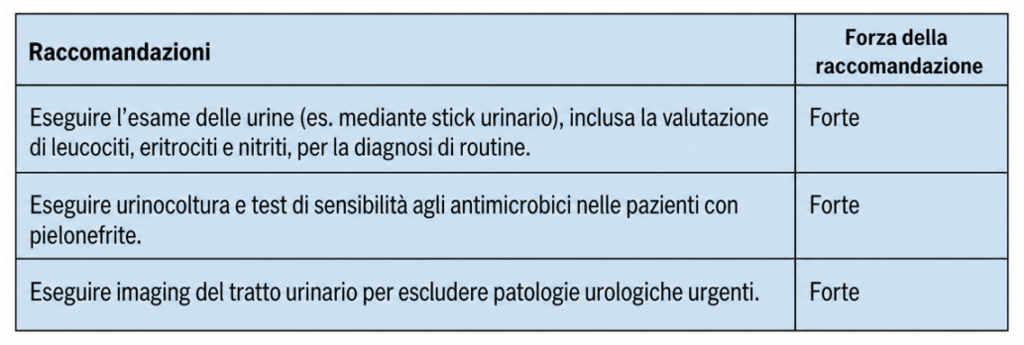
Il terrore delle forme sistemiche: quando sospettiamo la Pielonefrite?
Anche in questo caso non si sono verificati cambiamenti, si ricordano gli aspetti clinici centrali, con o senza i sintomi delle forme localizzate:
- Febbre>38°
- Brividi
- Dolore al fianco
- Nausea
- Vomito
- Dolore all’angolo costo-vertebrale
Rimane mandatoria la necessità d’esecuzione di Urinocoltura (UC) e dell’individuazione precoce dei possibili fattori di rischio per la progressione verso Urosepsi.
Per quanto concerne il trattamento, occorre considerare fluorochinolonici e cefalosporine; tuttavia, una considerazione interessante andrebbe fatta sulla durata del trattamento, in quanto se è vero che confrontando trattamenti più brevi con quelli più lunghi non si evidenziano successi terapeutici migliori, allo stesso tempo cicli di durata minore si associano spesso a recidive più frequenti
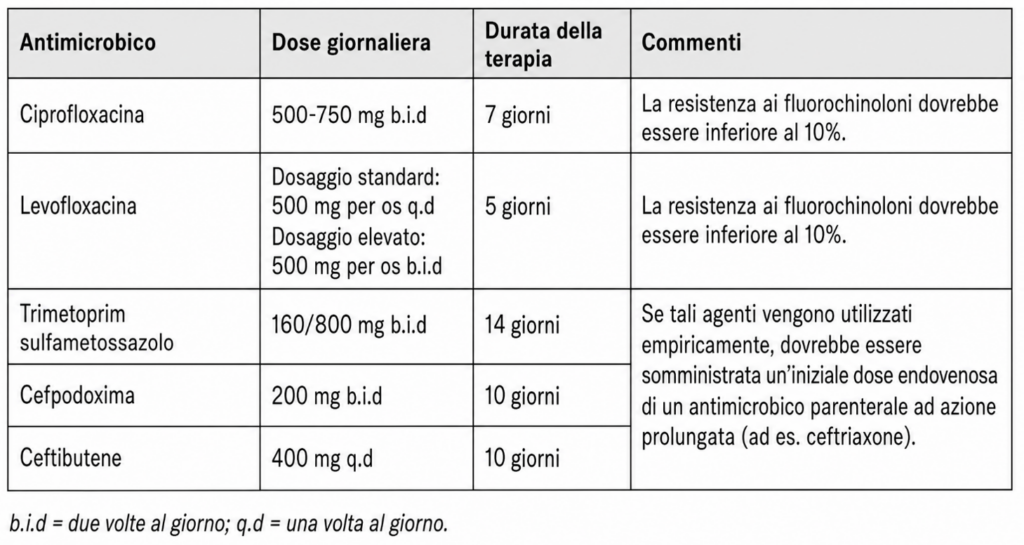
Che fare nelle forme sistemiche?
Nel riconoscere una forma sistemica, occorre ricordare che all’interno di queste rientrano le pielonefriti, le prostatiti acute e le urosepsi.
Nel caso della donna risulta centrale l’esame obiettivo pelvico per escludere problematiche ginecologiche, mentre nell’uomo sarebbe utile eseguire esplorazione rettale nel sospetto di prostatiti.
E’ consigliabile Iniziare una terapia antibiotica empirica ad ampio spettro nel più breve tempo possibile, dopo aver eseguito urinocoltura ed eventualmente valutare i fattori di rischio che possano portare ad una prognosi più infausta e quindi all’ospedalizzazione.
La durata della terapia varia dai 5 ai 10gg, secondo la risposta clinica ed in base alla molecola che utilizziamo, tuttavia eccezion fatta per il trattamento prolungato nell’uomo ove la terapia abbreviata non ha mostrato superiorità rispetto a quella long course, si tende a favoreggiare regimi di trattamento brevi e nel caso di buona risposta nelle forme ospedaliere, di shiftare verso ab orali quando ottenuta una buona risposta nelle prime 48-72h.
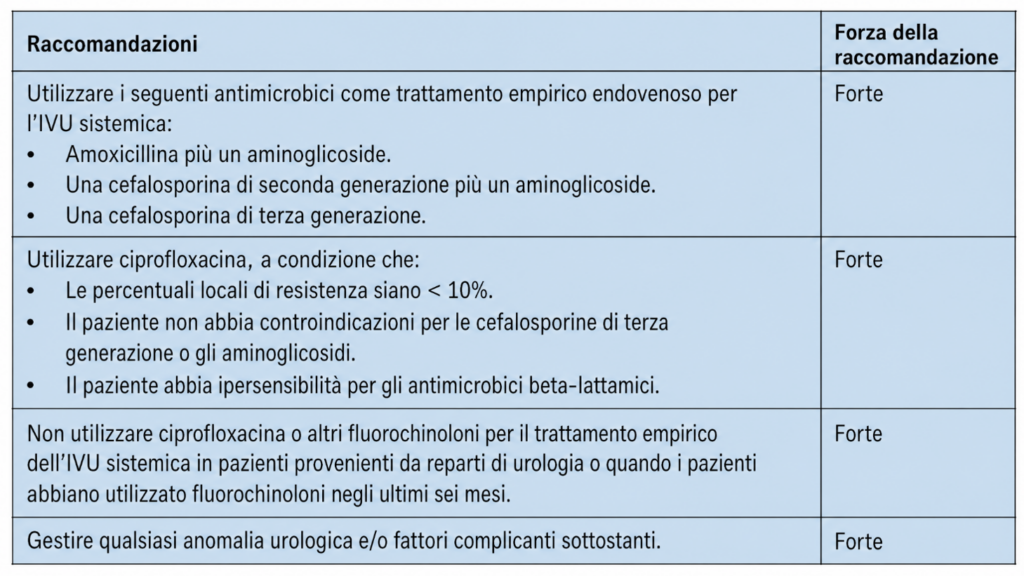
Gestire il paziente cateterizzato, quando trattare, quando eseguire UC?
L’indicazione rimane quella di trattare i pazienti con sintomi localizzati e/o sistemici, il trattamento antibiotico al cambio CV andrebbe verificato con UC, ma soprattutto si conferma la necessità di non trattare le batteriurie asintomatiche nei pz portatori di CV.
Uretriti e dintorni:
Seppur la stragrande maggioranza delle uretriti trovi la sua genesi nei rapporti sessuali, occorre ricordare che possiamo classificarle in forme infettive e non.
L’infezione che colpisce l’uretra anche in queste LG viene confermata dal sospetto clinico (disuria, alguria, dolore e prurito nell’uretra distale e nel meato esterno) ed ai segni tipici (perdite uretrali, eritema al meato uretrale esterno e linfoadenopatie inguinali).
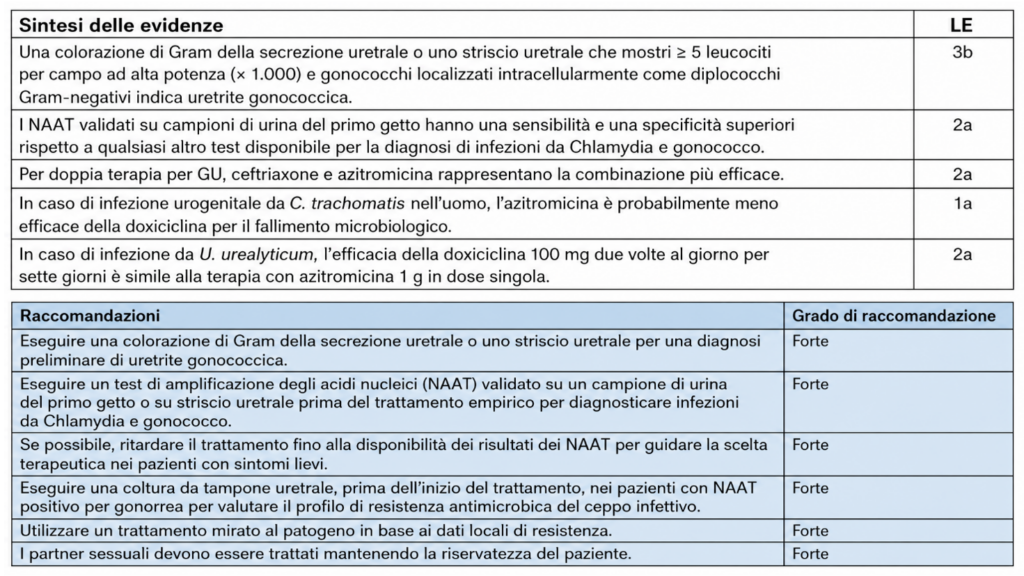
La differenziazione tra forme Gonococciche e non gonococciche sta nella rapida esecuzione di Gram stain sul secreto uretrale, il che ci permette di iniziare un eventuale trattamento empirico:
GU: Ceftriaxone 1-2gr Im o IV SD o Doxiciclina 100mg/bid 7gg o in caso di allergia Azitromicina 500mg/die 2-4gg
NGU: Doxiciclina 100mg/bid 7gg, in caso di allergia Azitromicina 500mg/die 2-4gg
Per la consultazione della scelta mirata in base ad esame colturale si rimanda invece alla consultazione completa delle LG.
Per quello che concerne le prostatiti batteriche le Linee Guida EAU 2026 confermano l’adozione della classificazione NIH, ma soprattutto rafforzano un principio già visto per le IVU: diagnosi mirata prima dell’antibiotico, stewardship antimicrobica e invio specialistico ragionato. Per il medico di medicina generale (MMG) e per lo specialista ambulatoriale territoriale, ecco i punti chiave da portare nella pratica quotidiana.
1. Classificazione NIH
| Tipo | Definizione | Frequenza territoriale |
| I | Prostatite acuta batterica | Rara, ma urgenza clinica |
| II | Prostatite cronica batterica | Bassa, ma spesso misconosciuta |
| III | Sindrome dolorosa pelvica cronica (CPPS) – IIIa infiammatoria / IIIb non infiammatoria | La forma di gran lunga più frequente in ambulatorio |
| IV | Prostatite infiammatoria asintomatica | Riscontro occasionale (es. biopsia, PSA) |
Il punto pratico: oltre il 90% dei pazienti che il MMG vede con sintomi “tipo prostatite” ha in realtà una CPPS (Tipo III), non un’infezione batterica. Questo riposiziona completamente l’uso dell’antibiotico.
2. Diagnosi sul territorio – cosa fare e cosa non fare
Prostatite acuta (Tipo I) – è l’unica vera urgenza territoriale:
- febbre, brividi, disuria, dolore perineale/pelvico, ritenzione urinaria
- urinocoltura prima dell’antibiotico
- stick urinario (esterasi leucocitaria + nitriti) come supporto diagnostico rapido
- non eseguire massaggio prostatico in fase acuta (rischio di batteriemia)
Forme croniche (Tipo II e III):
- NIH-CPSI (Chronic Prostatitis Symptom Index): strumento validato, gratuito, utilizzabile in ambulatorio per quantificare dolore, sintomi urinari e impatto sulla qualità di vita
- standard di localizzazione: test delle 4 tazze di Meares-Stamey
- alternativa pratica accettata dalle EAU: test delle 2 tazze pre/post-massaggio prostatico, più realistico in studio MMG
- valutazione delle MST (NAAT su urina del primo getto / tampone) nei pazienti più giovani o con fattori di rischio
Occorre pensare a complicanze in caso di dolore intenso e persistente, febbre che non risponde a 48–72 h di terapia adeguata. In tal caso possiamo sospettare un ascesso prostatico
3. Terapia antibiotica – la stewardship arriva anche in prostata
Prostatite acuta batterica (Tipo I)
- Terapia empirica con buona penetrazione prostatica;
- fluorochinoloni (ciprofloxacina, levofloxacina) restano efficaci ma vanno usati con criterio, vista la limitazione EMA/AIFA e i pattern di resistenza locale;
- in caso di sepsi o impossibilità di terapia orale → invio in PS / urologia per terapia endovenosa (cefalosporine di 3ª generazione ± aminoglicoside).
Prostatite cronica batterica (Tipo II)
- Fluorochinoloni (levofloxacina, ciprofloxacina, prulifloxacina) come prima scelta per penetrazione tissutale
- durata: 4–6 settimane
- in caso di Chlamydia trachomatis: azitromicina opzione comparabile
- in caso di Trichomonas vaginalis: metronidazolo 1,5 g/die per 7–14 giorni.
CPPS (Tipo III) – il vero salto culturale per il territorio:
- non è un’infezione, quindi non va trattata empiricamente con cicli ripetuti di antibiotico;
- approccio multimodale: alfa-litici, antinfiammatori, fitoterapici (Serenoa repens, quercetina, polline), fisioterapia del pavimento pelvico, supporto psicologico nei casi con impatto significativo sulla qualità di vita.
4. Criteri di invio allo specialista urologo
Il MMG dovrebbe inviare allo specialista quando:
- fallimento della terapia antibiotica di prima linea nella forma acuta dopo 48–72 h;
- sospetto ascesso prostatico (febbre persistente, dolore severo, sepsi);
- recidive dopo ciclo adeguato nella prostatite cronica batterica;
- CPPS resistente al trattamento multimodale di primo livello;
- dubbio diagnostico tra prostatite cronica e altre cause di dolore pelvico cronico (vescica iperattiva, sindrome della vescica dolorosa, patologia neurologica, dolore miofasciale del pavimento pelvico).
La nuova inclusione delle forme fungine:
La prevalenza di quest’ultime nel setting territoriale non supera l’1%, inoltre solo dal 2 all’11% si presenta con sintomi associabili ad IVU. Il patogeno che viene riscontrato con maggiore frequenza risulta essere la Candida Albicans 50-70%
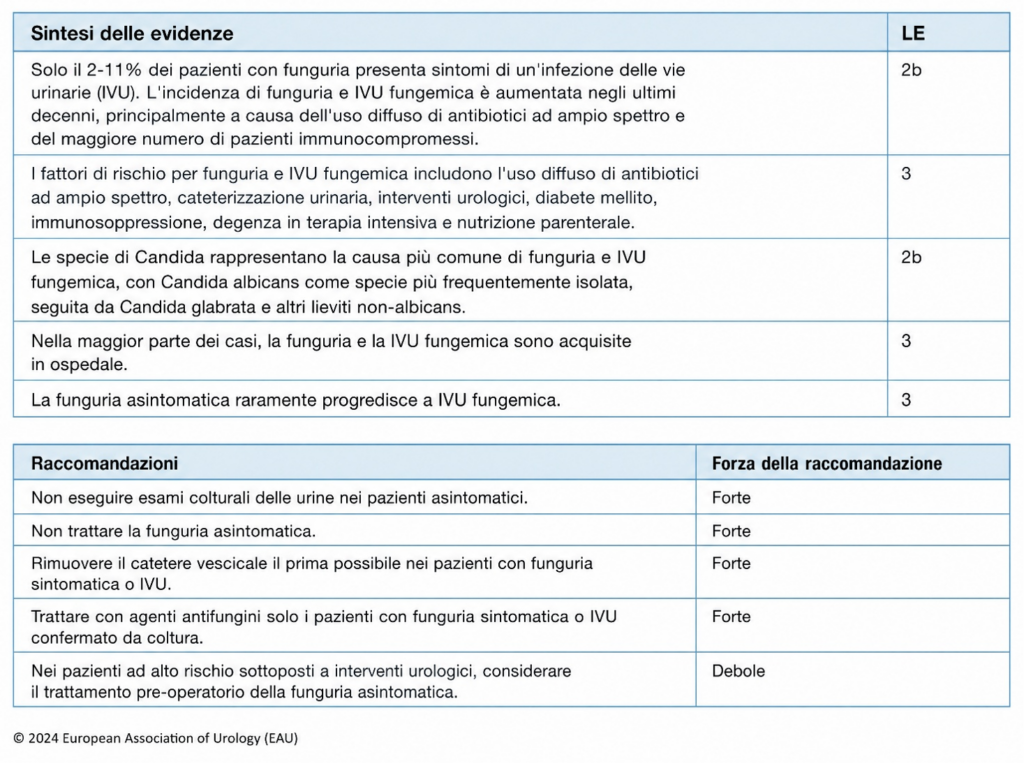
La gestione delle Urinocolture positive asintomatiche (ABU):
Concludiamo la stesura di questa review riportando la definizione di ABU che rappresenta la positività di un’urinocoltura nell’uomo con UFC≥10⁵ ed in due campioni nella donna, in assenza di clinica.
Ad oggi ci troviamo spesso nel nostro setting a dover prendere decisioni in casi clinici complessi, in pazienti complessi e con pochi dati laboratoristici; pertanto, si ritiene utile ricordare alcuni punti salienti, in particolare una wish list al negativo, vale a dire una serie di indicazioni a non eseguire UC:
- Non eseguire urinocolture di controllo al termine di un trattamento per verifica della negativizzazione
- Non eseguire in donne in assenza di FDR
- Non eseguire in pazienti con DM ben controllato
- Non eseguire in default in pz istituzionalizzati sopra i 65y
- Non eseguire in donne in menopausa
- Non eseguire in trapiantati renali
- Non eseguire prima d’interventi ortopedici di artroplastica
- Non eseguire in paziente con disfunzioni urologiche o che hanno subito interventi ricostruttivi
- Ambigua è la posizione nei confronti delle batteriurie precedenti interventi cardiovascolari, dove il livello di raccomandazione è basso, per cui si rimanda ad un allineamento con i protocolli aziendali regionali e locali
Il non eseguire in questo caso rappresenta anche il non trattare queste condizioni, riducendo sensibilmente l’utilizzo inappropriato di ab terapia e contribuendo in maniera sensibile alla futura e complessa lotta all’antimicrobico resistenza.
Conclusioni finali:
Il cambio di prospettiva introdotto dalle Linee Guida EAU 2026 non è una semplice revisione terminologica: rappresenta una vera riscrittura del modello mentale con cui clinici, microbiologi e farmacisti ospedalieri affrontano le infezioni urinarie. E questo riposizionamento ha un impatto diretto, e strategico sulla lotta all’antibiotico-resistenza (AMR).
Andiamo per punti:
1. Dalla dicotomia “complicata/non complicata” alla logica “localizzata vs sistemica”
Per anni la classificazione uUTI / cUTI (uncomplicated / complicated) ha funzionato da “interruttore terapeutico”: bastava la presenza di un catetere, di un’anomalia anatomica o del sesso maschile per far scattare in automatico antibiotici ad ampio spettro, durata lunga, terapia endovenosa.
Il risultato? Una sovra-esposizione antibiotica strutturale, soprattutto a fluorochinoloni e cefalosporine di terza generazione, in pazienti che spesso avevano solo una cistite con un fattore di rischio sullo sfondo.
Il modello EAU 2026, IVU localizzata (es. cistite) vs IVU sistemica (febbre, brividi, pielonefrite, prostatite), sposta la decisione clinica dal “contesto del paziente” alla “biologia dell’infezione”. È un passaggio che, dal punto di vista della antimicrobial stewardship, ha tre conseguenze enormi:
- evita che un paziente con cistite + catetere venga trattato come una sepsi urinaria;
- consente di riservare gli antibiotici di seconda linea ai veri casi sistemici;
- riduce la pressione selettiva su organismi commensali e nosocomiali, vero motore dell’AMR.
2. I fattori di rischio diventano un modificatore, non un upgrade terapeutico
Nelle nuove tabelle EAU, i fattori di rischio (lattanti, anziani fragili, immunocompromessi, anomalie anatomiche, cateteri, calcoli, gravidanza, prolasso, ecc.) non riclassificano automaticamente l’infezione come “complicata”: vengono presentati come elementi da affrontare (should be addressed), non come trigger per spettro più ampio.
Questo è centrale per l’AMR perché significa che la presenza di un fattore di rischio non giustifica più, di per sé, l’escalation antibiotica. Si apre invece lo spazio per interventi non farmacologici e correttivi, sostituzione del catetere, rimozione del calcolo, correzione del residuo post-minzionale, estrogeni vaginali in postmenopausa, che riducono la causa, non solo l’effetto.
3. Le opzioni antibiotic-sparing passano da “alternativa marginale” a raccomandazione forte
Uno dei segnali più rilevanti delle EAU 2026 è la promozione, con forza “Forte”, dell’uso di approcci che riducono l’uso di antibiotici nella cistite acuta e nella prevenzione delle recidive: FANS sintomatici nei casi selezionati, fitoterapici (Centaurii herba, Levistici radix, Rosmarini folium; xiloglucano + ibisco + propoli), D-mannosio (con evidenze contraddittorie), ippurato di metenamina, probiotici, estrogeni vaginali.
Tradotto sull’AMR significa:
- meno cicli antibiotici per episodio,
- riduzione della pressione selettiva su E. coli, Klebsiella, Proteus — proprio le specie in cui ESBL e carbapenemasi stanno crescendo più rapidamente.
4. Durate più brevi, de-escalation esplicita, scoraggiamento dei fluorochinoloni empirici
La nuova classificazione abilita inoltre e questo è il vero impatto AMR a breve termine, durate di terapia più brevi (es. 1 giorno per fosfomicina, 3 giorni per cotrimossazolo nella cistite, 5 giorni per nitrofurantoina) e una raccomandazione forte a non usare ciprofloxacina in IVU sistemica empirica se il paziente proviene da reparti urologici o ha già assunto fluorochinoloni negli ultimi 6 mesi.
5. Perché questo cambio di prospettiva è, di fatto, una politica AMR?
Mettendo insieme i tasselli, le EAU 2026 fanno una cosa che le precedenti versioni non avevano osato fare: spostano l’antibiotico dal centro della decisione clinica al margine; strumento potente, ma usato solo quando l’infezione lo richiede davvero (IVU sistemica) o quando le strategie non antibiotiche hanno fallito (recidive).
Da un punto di vista di sanità pubblica, questo significa:
- minor selezione di ESBL, AmpC, carbapenemasi;
- ricaduta positiva sulla sostenibilità degli antibiotici di riserva (ceftolozano/tazobactam, ceftazidima/avibactam, meropenem/vaborbactam) per i pazienti che ne hanno realmente bisogno
- allineamento con le strategie OMS, ECDC e PNCAR italiano sull’uso prudente degli antimicrobici.
Il vero messaggio delle EAU 2026 non è “abbiamo cambiato la tabella delle definizioni” ma dimostrare come laclassificazione delle IVU non sia una scorciatoia per giustificare l’utilizzo di antibiotici più potenti ed ad ampio spettro, ma tornare a essere uno strumento clinico per decidere se servono davvero.
Questo, per la lotta all’AMR, vale molto più di una nuova molecola: vale una nuova cultura prescrittiva, codificata e condivisa a livello europeo
Alessandro Marchesi MMG Perugia
SIMG Umbria
Esperto in strategie di prevenzione e vaccinali
Bibliografia
1. Vallée, M. et al. Urological Infections EAU Guidelines On. (2026).
2. Trautner, B. W. et al. Clinical Practice Guideline by Infectious Diseases Society of America (IDSA): 2025 Guideline on Management and Treatment of Complicated Urinary Tract Infections: Introduction and Methods. (“Introduction and Methods Manuscript 7_14_25 – IDSA”) Clinical Infectious Diseases https://doi.org/10.1093/cid/ciaf459 (2025) doi:10.1093/cid/ciaf459.
3. Smaill, F. M. & Vazquez, J. C. Antibiotics for asymptomatic bacteriuria in pregnancy. Cochrane Database of Systematic Reviews vol. 2019 Preprint at https://doi.org/10.1002/14651858.CD000490.pub4 (2019).
4. Lodise, T. P. et al. Pivmecillinam for Treatment of Uncomplicated Urinary Tract Infection: New Efficacy Analysis. Clinical Infectious Diseases vol. 81 e285–e293 Preprint at https://doi.org/10.1093/cid/ciaf280 (2025).
5. Wykowski, R., Fuentefria, A. M. & de Andrade, S. F. Antimicrobial activity of clioquinol and nitroxoline: a scoping review. Archives of Microbiology vol. 204 Preprint at https://doi.org/10.1007/s00203-022-03122-2 (2022).
6. Williams, G., Hahn, D., Stephens, J. H., Craig, J. C. & Hodson, E. M. Cranberries for preventing urinary tract infections. Cochrane Database of Systematic Reviews 2023, (2023).
7. Xiong, Z., Gao, Y., Yuan, C., Jian, Z. & Wei, X. Preventive effect of cranberries with high dose of proanthocyanidins on urinary tract infections: a meta-analysis and systematic review. Frontiers in Nutrition vol. 11 Preprint at https://doi.org/10.3389/fnut.2024.1422121 (2024).